1, 4-dioxane là một hợp chất đã được biết đến như một chất gây ô nhiễm mới nổi. Có thể gây ra những ảnh hưởng tiêu cực đến sức khỏe con người. Cơ quan Đăng ký Chất độc và Bệnh tật Hoa Kỳ (ATSDR) tuyên bố rằng việc tiếp xúc với 1, 4-dioxane ở mức cao có thể gây tổn thương gan và thận. 1,4-dioxane cũng được dự đoán một cách hợp lý là chất gây ung thư ở người. Dựa trên bằng chứng đầy đủ về khả năng gây ung thư ở động vật.
US EPA cũng đã phân loại 1,4-dioxane là “có khả năng gây ung thư cho người”. Nghiên cứu gần đây đã đánh giá phơi nhiễm qua nước uống và thực phẩm. Tạo ra một bức tranh toàn cảnh về khả năng gây ung thư.
Phơi nhiễm 1,4-dioxane xảy ra từ nhiều nguồn khác nhau. Nó được sử dụng làm chất ổn định trong một số dung môi clo hóa.
Có thể được tìm thấy trong nhiều sản phẩm được biết là sử dụng dung môi clo hóa như:
Dioxane cũng được sử dụng làm dung môi để tạo điều kiện thuận lợi cho các phản ứng SN2 trong quá trình tổng hợp hóa học vì bản chất không proton của nó. Dioxane cũng là sản phẩm phụ của các phản ứng ethoxyl hóa. Nhiều trong số đó được thực hiện thường xuyên là các sản phẩm mỹ phẩm có chứa natri laureth sulfat.
Thuốc thử này phổ biến trong các sản phẩm mỹ phẩm. Có thể phát hiện được lượng 1,4-dioxane được tìm thấy trong gần 57% dầu gội trẻ em và 97% thuốc duỗi tóc.
FDA và Ủy ban Khoa học về An toàn Người tiêu dùng của EU, dựa trên lời khuyên của Cơ quan Hợp tác Quốc tế về Quy định Mỹ phẩm (ICCR), đã khuyến nghị giới hạn đối với 1,4-dioxane trong các sản phẩm mỹ phẩm thành phẩm là dưới 10 ppm. Vì nguồn chính của 1,4-dioxane hiện là sản phẩm mỹ phẩm. Không có gì ngạc nhiên khi nó có thể được tìm thấy trong cả nước uống và nước ngầm.
Nhật Bản đã quan sát thấy nồng độ trong nước mặt lên tới 42,8 μg/L và tìm thấy tới 79 μg/L trong các mẫu nước ngầm. Trong trường hợp này, một mối tương quan cao đã được quan sát với sự hiện diện của 1,1,1-trichloroethane. 1,4-Dioxane được tìm thấy ở nồng độ 0,2–1,5 μg/L trong các mẫu nước máy từ sáu thành phố ở Kanagawa, Nhật Bản, vào năm 1995–1996.
Ở Hoa Kỳ, 1, 4-dioxane được đưa vào Quy tắc giám sát chất gây ô nhiễm không được kiểm soát lần thứ ba (UCMR-3). Một danh sách các hợp chất gây ô nhiễm ứng cử viên dựa trên độc tính và sự xuất hiện.
Danh sách 30 hợp chất được theo dõi trong các nguồn cung cấp nước công cộng lớn và các nguồn cung cấp nước nhỏ. được chọn để hiểu rõ hơn về sự xuất hiện và cường độ trong nước uống để hỗ trợ quyết định xem quy định có được đảm bảo hay không.
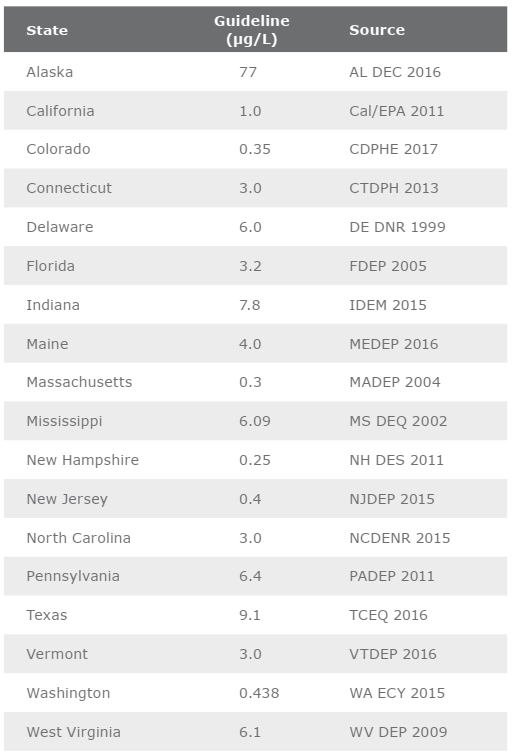
Kết quả của UCMR-3 không dẫn đến mức tối đa theo quy định mức độ gây ô nhiễm là 1, 4-dioxane. Nhưng một số tiểu bang đang bắt đầu thiết lập các quy định. Các quy định này có thể được quan sát trong Bảng 1 2. Các đánh giá rủi ro của EPA chỉ ra rằng nồng độ trong nước uống thể hiện mức rủi ro ung thư 1 x 10 -6 đối với 1,4-dioxane là 0,35 μg/L.
Một số lo ngại đã nảy sinh về phép đo 1, 4-dioxane trong các mẫu nước do dioxane có ái lực cao với nước. Hợp chất này có thể hòa tan hoàn toàn trong nước. Và mặc dù nó dễ bay hơi nhưng rất khó để loại bỏ khỏi nước.
Việc đánh giá 1,4-dioxane có thể được thực hiện bằng một số phương pháp EPA hiện có của Hoa Kỳ. Sử dụng chiết xuất để loại bỏ 1,4-dioxane khỏi nước để đo GC/MS. Nhưng các phương pháp này đã được chứng minh là có giới hạn phát hiện kém hơn so với mong muốn.
US EPA phương pháp 522 từ chương trình nước uống quy định chiết xuất pha rắn (SPE) và phân tích GC/MS. Bằng cách sử dụng giám sát ion đơn (SIM) và là phương pháp thành công nhất cho đến nay. Lưu ý ứng dụng này sẽ đánh giá hiệu suất của hệ thống chiết xuất pha rắn tự động Biotage ® Horizon 5000 kết hợp với US EPA Method 522.
Quá trình chiết được thực hiện bằng hệ thống chiết pha rắn tự động Biotage ® Horizon 5000. Sử dụng chương trình chiết được trình bày trong Bảng 2. Cỡ mẫu nước 500 mL được chiết ở độ pH trung tính.
Để cải thiện hiệu suất của phương pháp, vật tư tiêu hao được sử dụng cho lưu ý ứng dụng này là hộp than dừa 3 gam, 6 cc. Thay đổi này không chỉ thể hiện tốc độ thu hồi tối ưu mà còn cho phép vận hành hệ thống 5000 ở tốc độ nạp mẫu là 3.
Thay đổi vận hành này cho phép tăng tốc độ nạp mẫu lên khoảng 25 mL/phút từ 10 mL/phút. Và là phương pháp tuân thủ do ngôn ngữ trong phần 1.6 của EPA phương pháp 522. Điều này tiết kiệm được khoảng 20 phút cho mỗi mẫu.
Bước phân tích được thực hiện bằng GC/MS ở chế độ ion đơn (SIM) để có độ nhạy tốt nhất. Các điều kiện cho Agilent 7890A GC kết hợp với khối phổ kế Agilent 5975C được trình bày trong Bảng 3.
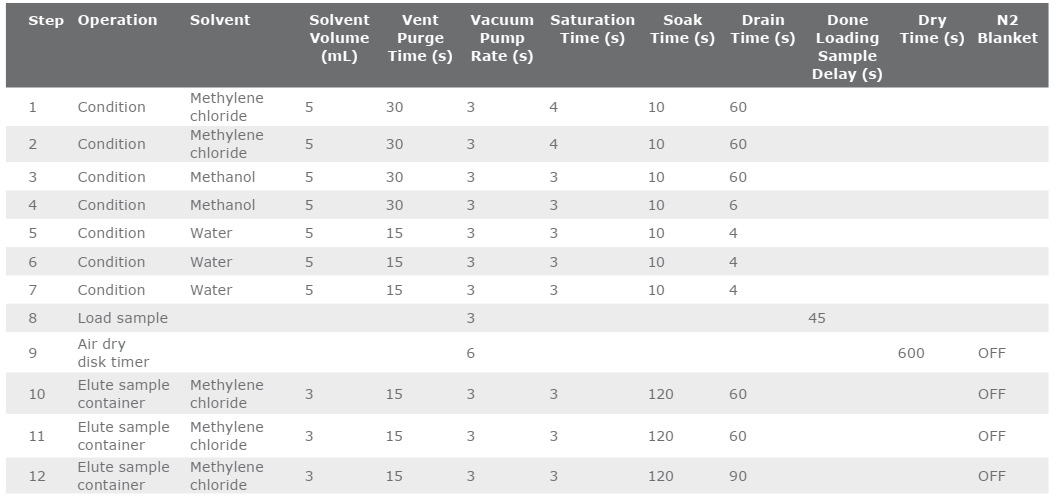
Bảng 2. Chương trình chiết xuất được sử dụng trên hệ thống Biotage ® Horizon 5000.
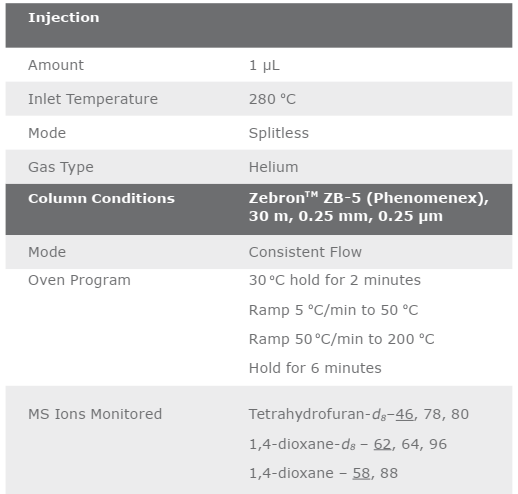
Bảng 3. Thông số GC/MS.

2 thiết bị chiết Biotage ® Horizon 5000 được trang bị hộp carbon để chiết. Cả hai trình trích xuất đều được điều khiển bằng PC ở giữa hình ảnh.
Bảng 6 trong EPA Method 522 liệt kê các yêu cầu trình diễn ban đầu về khả năng (IDC). Cũng như các yêu cầu kiểm soát chất lượng đối với phân tích 1,4-dioxane. Bảng 7 trong Phương pháp 522 liệt kê các yêu cầu kiểm soát chất lượng liên tục phải liên tục được đáp ứng.
Phương pháp nêu rõ rằng nền thấp của hệ thống và thuốc thử phải được xác định bằng cách kiểm tra mẫu trắng thuốc thử phòng thí nghiệm (LRB). Chất thay thế được thêm vào mẫu trắng thuốc thử để đảm bảo rằng quá trình chiết được thực hiện theo tiêu chuẩn của phương pháp.
Các nhiễu 1, 4-dioxane và nền phải nhỏ hơn hoặc bằng 1/3 MRL để tiếp tục đáp ứng các yêu cầu của IDC. Kết quả cho một mẫu LRB được trình bày trong Bảng 4.

Bảng 4. Phương pháp blank.
Một bộ 4 mẫu trắng tăng cường trong phòng thí nghiệm (LFB) đã được trích xuất trên Biotage ® Horizon 5000 để xác định trình diễn ban đầu về độ chụm (IDP). Độ chính xác (độ lệch chuẩn tương đối (RSD)) của cả bốn mẫu phải ≤20%. Các kết quả về độ chụm được trình bày trong Bảng 5.
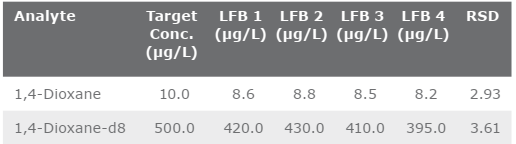
Bảng 5. Trình diễn ban đầu về độ chụm (IDP)
Trình diễn ban đầu về độ chính xác (IDA), được trình bày trong Bảng 6. Sử dụng cùng bốn LFB đã được sử dụng để xác định IDP. Phương pháp xác định rằng để chứng minh độ chính xác. Độ phục hồi trung bình của LFB phải là +/- 20% giá trị thực. Giá trị thực của từng mẫu trong số bốn mẫu là 10 µg/L.
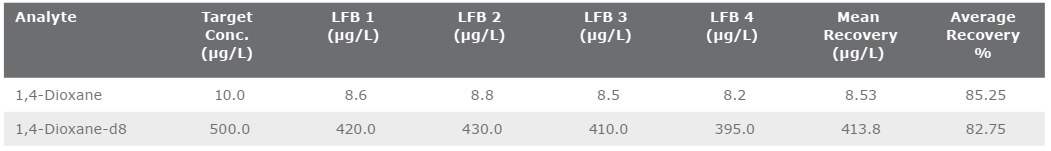
Bảng 6. Trình diễn ban đầu về độ chính xác (IDA)
LFB đã được trích xuất để xác nhận mức báo cáo tối thiểu (MRL). Và xác định một nửa phạm vi cho khoảng thời gian dự đoán của kết quả (HRPIR). Tập dữ liệu này cung cấp một RL cho thiết bị chiết xuất pha rắn tự động SPE Biotage® Horizon 5000. Dữ liệu MRL và HRPIR được trình bày trong Bảng 7.
Phương trình tính HRPIR như sau:
HRPIR = 3.963 S
Trong đó S là độ lệch chuẩn và 3,963 là giá trị không đổi trong 7 lần lặp lại.
Dữ liệu từ Bảng 7 cũng được sử dụng để xác nhận khoảng dự đoán trên và dưới của kết quả (PIR). Hai giới hạn này phải được đáp ứng để xác nhận rằng MRL hợp lệ. Giới hạn PIR trên phải nhỏ hơn hoặc bằng 150% trong khi giới hạn PIR dưới phải lớn hơn hoặc bằng 50%. Dữ liệu cho các giới hạn PIR trên và dưới được trình bày trong Bảng 8. Các phương trình tính PIR trên và PIR dưới như sau:
(Trung bình + HRPIR / Nồng độ tăng cường) *100
Thấp hơn:
(Trung bình – HRPIR / Nồng độ tăng cường) *100
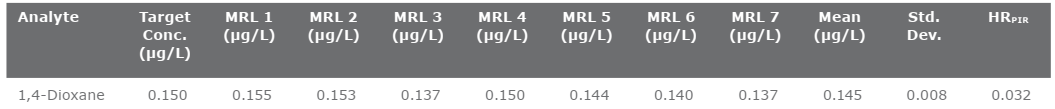
Bảng 7. Dữ liệu MRL cho bảy lần lặp lại được sử dụng để tính HRPIR . Các giá trị được báo cáo (μg/L) chiếm thể tích ban đầu 500 mL và thể tích dịch chiết cuối cùng là 10 mL
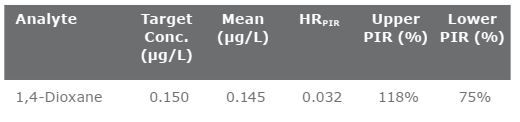
Bảng 8. Tính toán giới hạn PIR trên và dưới
Giới hạn phát hiện phương pháp (MDL) (tùy chọn đối với IDC) đã được tính toán bằng cách sử dụng quy trình trong 40CFR, phần 136 cho MDL ban đầu. Tám LFB được thêm vào ở nồng độ thấp (0,15 μg/L) và được chiết xuất qua Biotage ® Horizon 5000 trong khoảng thời gian một tháng.
Độ lệch chuẩn của tám lần lặp lại được nhân với giá trị T của Sinh viên là 2,998 để tính MDL. Kết quả của nghiên cứu MDL được trình bày trong Bảng 9.
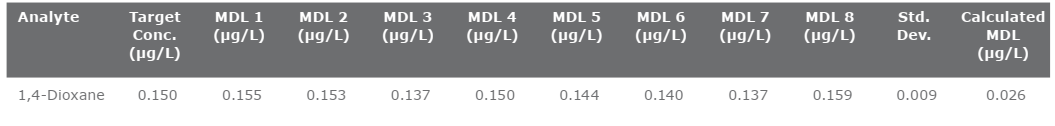
Bảng 9. Xác định giới hạn phát hiện MDL
Phương pháp 522 quy định rằng lô phân tích chứa từ 10–20 mẫu phải chứa mẫu trắng tăng cường phòng thí nghiệm (LFB) để kiểm tra kiểm soát chất lượng. Nồng độ của LFB nên xoay vòng giữa nồng độ thấp, trung bình và cao. Tiêu chí chấp nhận đối với LFB thấp là +/-50% giá trị thực trong khi LFB trung bình và cao phải nằm trong khoảng +/-30% giá trị thực. Dữ liệu về ba LFB, một ở mỗi nồng độ, được trình bày trong Bảng 10
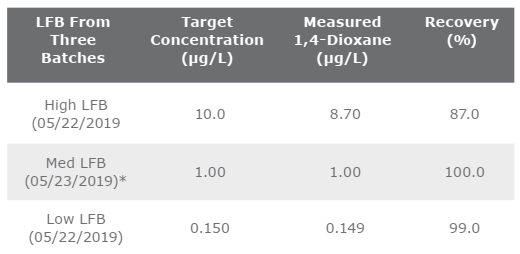
Bảng 10. Các giá trị thu hồi đối với các mẫu trắng tăng cường trong phòng thí nghiệm
Các hộp mực ba gam hoạt động cực kỳ tốt và vượt qua tất cả các yêu cầu của IDC và QC liên tục. Hộp mực ba gam cho phép xử lý mẫu nhanh hơn . Vì thể tích chất hấp phụ lớn hơn cho phép kéo mẫu qua nhanh hơn đồng thời ngăn chặn sự đột phá. Sự phục hồi đo được của hai mươi chất thay thế được trình bày trong Hình 2.
Một mẫu thử nghiệm hiệu suất mù (PT) đã được phân tích để đảm bảo rằng quy trình chiết xuất. Cũng như phương pháp phân tích, có khả năng định lượng. Một mẫu đã được nhận từ một nhà cung cấp được công nhận. Và được chiết xuất bằng Biotage® Horizon 5000. Các kết quả cũng như tiêu chí chấp nhận được trình bày trong Bảng 11.

Bảng 11. Giá trị phục hồi cho mẫu kiểm tra hiệu suất
Ứng dụng này chứng minh rằng phương pháp EPA 522 có thể được thực hiện thành công trong phòng thí nghiệm bằng cách sử dụng hệ thống chiết pha rắn tự động SPE Biotage® Horizon 5000.
4 mẫu LFB đã được phân tích về độ chính xác và độ chính xác. Mang lại giá trị thu hồi trung bình là 85,25% với RSD là 2,93%. Cả hai giá trị đều đáp ứng các tiêu chí chấp nhận của phương pháp. Các yêu cầu kiểm soát chất lượng theo lô được đặt ra theo phương pháp EPA. Dễ dàng được đáp ứng bằng phương pháp chiết xuất này.
Việc tự động hóa phương pháp này cung cấp ít sự can thiệp của nhà phân tích hơn. Giúp giảm bất kỳ sự nhiễm bẩn bên ngoài nào có thể xảy ra.
Thể tích dịch chiết cuối cùng 10 mL giúp loại bỏ mọi tổn thất do bay hơi trong khi lớp chất hấp phụ lớn hơn. Cho phép tốc độ dòng chảy nhanh hơn với hiệu suất tốt hơn. Tất cả những yếu tố này giúp tăng năng suất đồng thời dễ dàng đáp ứng tất cả các yêu cầu kiểm soát chất lượng đối với EPA Method 522.
Hãy liên hệ đến chúng tôi để được tư vấn và báo giá tốt nhất.
Email của chúng tôi: info@tegent.com.vn
Zalo: 0987445016
Xem thêm sản phẩm Biotage Horizon tại đây
Bài viết tham khảo tại đây
Xem thêm video về sản phẩm của Tegent tại đây